4. Если в таблице нет цифры, соответствующей найденной плотности, то последнюю вычисляют методом интерполяции по двум ближайшим величинам.
Например , плотность раствора HСl равна 1,032 г/мл.
Берут значения плотности больше и меньше измеренной, и соответствующие им концентрации. Находят разности:
При увеличении плотности на 0,01 процентное содержание соляной кислоты увеличивается на 2%. Найденная плотность меньше наибольшего значения на 1,038 - 1,032 = 0,006. Находят процентное содержание, соответствующее плотности 0,006:
Х = (2 · 0,006) : 0,01 = 1,2 (%).
Вычитая эту величину из наибольшего значения, получают искомую величину:
8% - 1,2% = 6,8%.
5. Зная процентное содержание HCl, вычисляют объем концентрированного (исходного) раствора, который необходимо взять для приготовления 0,1N раствора HCl. Объем исходного раствора рассчитывают по формуле:
V – объем концентрированного (исходного) раствора HCl, мл;
С м – молярная концентрация раствора (С м = С N ·f), моль/л;
V к – объем мерной колбы, мл;
М – молекулярная масса вещества, г/моль;
ρ - плотность исходного раствора, г/мл;
ω – процентная концентрация исходного раствора, %.
Например , необходимо приготовить 200 мл 0,1N раствора HCl, тогда
Следовательно, для приготовления 200мл 0,1N (С м = 0,1N·1, т.к. f=1) раствора HCl нужно взять 10,4 мл соляной кислоты плотностью 1,032 г/мл.
5. Мерной пипеткой с точностью до десятых долей мл отмеривают рассчитанный исходный концентрированный раствор HCl, переносят в мерную колбу нужного объема и доводят до метки дистиллированной водой так, чтобы нижний край мениска касался метки.


6. Закрывают колбу пробкой и тщательно перемешивают раствор, переворачивая колбу несколько раз. Полученный таким образом раствор является приблизительно 0,1N. Точная нормальность такого раствора устанавливается с помощью титриметрических анализов.
7. Оформляют работу. Формулируют выводы.
Автор Химическая энциклопедия г.р. Н.С.ЗефировСОЛЯНАЯ КИСЛОТА
(хлористоводородная кислота, хлороводородная кислота), раствор НCl в воде-бесцв. жидкость
с резким запахом; рильная одноосновная кислота. Хлористый водород НCl (мол.
м. 36,461)-бесцв. газ с резким запахом, во влажном воздухе сильно дымит; длина
связи H-Cl 0,1274 нм, m
3,716 10 -30 Кл м, энергия диссоциации
427,77 кДж/моль; температура кипения -85,1 °С (бесцв. легко подвижная жидкость), т.
пл. -114,22 °С; кристаллизуется в кубич. решетке, ниже -174,15 °С существует
ромбич. модификация; тройная точка -114,22 °С; плотность по воздуху 1,2679;
Г крнт 51,4°С, p крит 8,258 МПа, d крит
0,42 г/см 3 ;
-92,31 кДж/моль, D
H пл 1,9924 кДж/моль (-114,22°С),
D
H исп 16,1421 кДж/моль (-8,05°С);186,79
Дж/(моль К); давление пара (Па): 133,32 10 -6 (-200,7°С), 2,775 10 3
(-130,15°С), 10,0 10 4 (-85,1 °С), 74,0 10 4
(-40°С), 24,95 10 5 (О °С), 76,9 10 5 (50 °С);
уравение температурной зависимости давления пара lgp(кПа) = -905,53/Т+
1,75lgT- -500,77 10 -5 T+3,78229 (160-260 К); коэффициент сжимаемости
0,00787; g
23 мН/см (-155°С); r
0,29 10 7 Ом м (-85°С),
0,59 10 7 (-114,22°С). См. также табл. 1.
Растворимость НCl в углеводородах
при 25 °С и 0,1 МПа (мол. %): в пентане-0,47, гексане-1,12, гептане-1,47,
октане-1,63. Растворимость НCl в алкил- и арилгалогенидах невелика, например 0,07 моль/моль
для С 4 Н 9 Cl. Растворимость в интервале от -20 до 60° С
уменьшается в ряду дихлорэтан-три-хлорэтан-тетрахлорэтан-трихлорэтилен. Растворимость
при 10°С в ряде спиртов составляет примерно 1 моль/моль спирта, в эфирах
карбоновых кислот 0,6 моль/моль, в карбо-новых кислотах 0,2 моль/моль. В простых эфирах
образуются устойчивые аддукты R 2 O НСl. Растворимость НCl в расплавах
хлоридов подчиняется закону Генри и составляет для КСl 2,51 10 -4
(800°С), 1,75 10 -4 моль/моль (900°С), для NaCl 1,90 10 -4
моль/моль (900 °С).
Соляная кислота. Растворение
НСl в воде-сильно экзо-термодинамически процесс, для бесконечно разбавленый водного раствора D
H 0
растворения НСl -69,9 кДж/моль,
иона Сl - -
167,080 кДж/моль; НCl в воде полностью ионизирован. Растворимость НCl в воде зависит
от температуры (табл. 2) и парциального давления НCl в газовой смеси. Плотность СОЛЯНАЯ КИСЛОТА
к. различные концентрации и h
при 20 °С представлены в табл. 3 и 4. С повышением
температуры h
СОЛЯНАЯ КИСЛОТА к. понижается, например: для 23,05%-ной СОЛЯНАЯ КИСЛОТА к. при 25 °С h
1364мПа с, при 35 °С 1,170 мПа с.С.
к., содержащей h
молей воды на 1 моль НCl, составляет [кДж/(кг К)]:
3,136 (п = 10), 3,580 (п = 20), 3,902 (п =50), 4,036 (n
= 100), 4,061 (п = 200).



![]()
НCl образует с водой азеотропную
смесь (табл. 5). В системе HCl-вода существует три эвтектич. точки: - 74,7 °С
(23,0% по массе НСl); -73,0°С (26,5% НСl); -87,5°С (24,8% НCl, метастабильная
фаза). Известны кристаллогидраты НСl nН 2 О, где n =
8, 6 (температура плавления -40 °С), 4, 3 (температура плавления -24,4°С), 2 (температура плавления -17,7°С)
и 1 (температура плавления -15,35°С). Лед кристаллизуется из 10%-ной СОЛЯНАЯ КИСЛОТА к. при -20, из
15%-ной-при -30, из 20%-ной-при -60 и из 24%-ной-при -80°С. Растворимость галогенидов
металлов с увеличением концентрации НCl в СОЛЯНАЯ КИСЛОТА к. падает, что используют для их
высаливания.
Химические свойства. Чистый
сухой НСl начинает диссоциировать выше 1500°С, химически пассивен. Мн. металлы,
С, S, P не взаимодействие даже с жидким НCl. С нитридами, карбидами, боридами,
сульфидами реагирует выше 650 °С, с гидридами Si, Ge и В-в присутствии АlСl 3 ,
с оксидами переходных металлов-при 300 °С и выше. Окисляется О 2
и HNO 3 до Сl 2 , с SO 3 дает ClSO 3 H.
О реакциях с органическое соединениями см. Гидрогалогенирование.
СОЛЯНАЯ КИСЛОТА к. химически
весьма активна. Растворяет с выделением Н 2 все металлы, имеющие отрицат.
нормальный потенциал, со
многие оксидами и гидроксидами металлов образует хлориды, выделяет свободный кислоты из
таких солей, как фосфаты, силикаты, бораты и др.
Получение.
В промышленности
НCl получают следующей способами-сульфатным, синтетич. и из абгазов (побочных газов)
ряда процессов. Первые два метода теряют свое значение. Так, в США в 1965 доля
абгазной СОЛЯНАЯ КИСЛОТА к. составляла 77,6% в общем объеме производства, а в 1982-94%.
Произ-во СОЛЯНАЯ КИСЛОТА к. (реактивной,
полученной сульфатным способом, синтетич., абгазной) заключается в получении
НCl с последующей его абсорбцией водой. В зависимости от способа отвода теплоты
абсорбции (достигает 72,8 кДж/моль) процессы разделяются на изотермодинамически, адиабатич.
и комбинированные.
Сульфатный метод основан
на взаимодействие NaCl с конц. H 2 SO 4 при 500-550 °С. Реакц.
газы содержат от 50-65% НCl (муфельные печи) до 5% НСl (реактор с кипящим слоем).
Предложено заменить H 2 SO 4 смесью SO 2 и О 2
(температура процесса около 540 °С, катализатор-Fе 2 О 3).
В основе прямого синтеза
НCl лежит цепная реакция горения: Н 2
+ Сl 2 2НСl+184,7кДж
Константа равновесия К р рассчитывается по уравению: lgK p
= 9554/T- 0,5331g T+ 2,42.
Реакция инициируется светом,
влагой, твердыми пористыми (древесный уголь, пористая Pt) и нек-рыми минеральных
веществами (кварц, глина). Синтез, ведут с избытком Н 2 (5-10%) в камерах
сжигания, выполненных из стали, графита, кварца, огнеупорного кирпича. Наиб.
современной материал, предотвращающий загрязнение НСl,-графит, импрегнированный фе-ноло-формальд.
смолами. Для предотвращения взрывного характера горения реагенты смешивают непосредственно
в факеле пламени горелки. В верх. зоне камер сжигания устанавливают теплообменники
для охлаждения реакционное газов до 150-160°С. Мощность современной графитовых печей
достигает 65 т/сут (в пересчете на 35%-ную СОЛЯНАЯ КИСЛОТА к.). В случае дефицита Н 2
применяют различные модификации процесса; например, пропускают смесь Cl 2
с водяным паром через слой пористого раскаленного угля:
2Сl 2 + 2Н 2 О
+ С :
4НCl + СО 2 + 288,9 кДж
Температура процесса (1000-1600
°С) зависит от типа угля и наличия в нем примесей, являющихся катализаторами
(например, Fe 2 O 3). Перспективно использование смеси СО с
парами воды:
СО + Н 2 О + Сl 2
:
2НCl + СО 2
Более 90% СОЛЯНАЯ КИСЛОТА к. в развитых
странах получают из абгаз-ного НCl, образующегося при хлорировании и дегидрохло-рировании
органическое соединений, пиролизе хлорорганическое отходов, хлоридов металлов, получении калийных
нехлорир. удобрений и др. Абгазы содержат различные количества НCl, инертные примеси
(N 2 , H 2 , СН 4), малорастворимые в воде органическое
вещества (хлорбензол, хлорметаны), водорастворимые вещества (уксусная кислота, хлораль),
кислые примеси (Сl 2 , HF, О 2) и воду. Применение изотермодинамически
абсорбции целесообразно при низком содержании НCl в абгазах (но при содержании
инертных примесей менее 40%). Наиб. перспективны пленочные абсорберы, позволяющие
извлекать из исходного абгаза от 65 до 85% НCl.
Наиб. широко применяют
схемы адиабатич. абсорбции. Абгазы вводят в ниж. часть абсорбера, а воду (или
разбавленную СОЛЯНАЯ КИСЛОТА к.)-противотоком в верхнюю. СОЛЯНАЯ КИСЛОТА к. нагревается до температуры кипения
благодаря теплоте растворения НСl. Изменение температуры абсорбции и концентрации НCl
дано на рис. 1. Температура абсорбции определяется температурой кипения кислоты соответствующей
концентрации (макс. температура-температура кипения азеотропной смеси-около 110°С).
На рис. 2 дана типовая
схема адиабатич. абсорбции НCl из абгазов, образующихся при хлорировании (например,
получение хлорбензола). НСl поглощается в абсорбере 1, а остатки малорастворимых
в воде органическое веществ отделяют от воды после конденсации в аппарате 2, доочищают в
хвостовой колонне 4 и сепараторах 3, 5 и получают товарную СОЛЯНАЯ КИСЛОТА к.

Рис. 1. Схема распределения
температур (кривая 1) и концентрации (кривая 2) НСl по высоте адиабатич. абсорбера.

Рис.2. Схема типовой адиабатич.
абсорбции НСl из абгазов: 1-адиабатич. абсорбер; 2 - конденсатор; 3, 5-сепараторы;
4-хвостовая колонна; 6-сборник органическое фазы; 7-сборник водной фазы; 8, 12-насосы;
9-отдувочная колонна; 10-теплообменник; 11-сборник товарной кислоты.
На рис. 3 дана типовая
схема получения СОЛЯНАЯ КИСЛОТА к. из абгазов с использованием комбинир. схемы абсорбции.
В колонне адиабатич. абсорбции получают СОЛЯНАЯ КИСЛОТА к. пониж. концентрации, но свободную
от органическое примесей СОЛЯНАЯ КИСЛОТА к. с повыш. концентрацией НСl производят в колонне изотермодинамически
абсорбции при пониж. температурах. Степень извлечения НCl из абгазов95-99% (при использовании
в качестве абсорбента разбавленый кислот) и практически полная-при использовании чистой
воды.
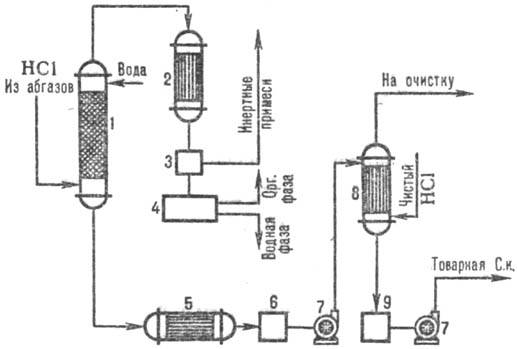
Рис. 3. Схема типовой комбинир.
абсорбции НCl из абгазов: 1 - колонна адиабатич. абсорбции; 2 - конденсатор;
3-отделитель газов; 4-сепаратор; 5-холодильник; 6, 9-сборники кислоты; 7-насосы;
8-изотермодинамически абсорбер.
Определяют НCl в воздухе
нефелометрически с образованием AgCl.
СОЛЯНАЯ КИСЛОТА к. применяют для получения
хлоридов Mn, Fe, Zn и др., для травления металлов, очистки поверхностей сосудов,
скважин от карбонатов, обработки руд, при производстве каучуков, глу-тамината Na,
соды, Сl 2 и т. д. Потребление СОЛЯНАЯ КИСЛОТА к. в Японии (тысяч т); химический промышленость
320,7, производство глутамината Na 99,8, производство соды 54,8, черная металлургия
50,0, целлюлозно-бумажная промышленость 22,2, прочие 80. НCl используют для
регенерации Сl 2 , в органическое синтезе (получение винилхлорида, алкилхлоридов
и т.д.), как катализатор (например, при получении дифенилолпропана, алкилирование
бензола).
Произ-во 31%-ной СОЛЯНАЯ КИСЛОТА к.
в СССР 1,52 млн. т (1986). НCl
и СОЛЯНАЯ КИСЛОТА к. токсичны, вызывают сильные ожоги слизистых оболочек, удушье, разрушают
зубы и т.д. ПДК НCl в воздухе рабочей зоны 5,0 мг/м 3 .
Литература: Якименко Л.
М., Пасманик М. И., Справочник по производству хлора, каустической соды и основных
хлорпродуктов, 2 изд., М., 1976; Левинский М. И., Мазанко А. Ф., Новиков И.
Н., Хлористый водород и соляная кислота, М., 1985. А. И. Торубаров.
Химическая энциклопедия. Том 4 >>
| Плотность, г/мл | Массовое содержание, % | Плотность, г/мл | Массовое содержание, % |
| 1,003 | 1,088 | ||
| 1,008 | 1,098 | ||
| 1,018 | 1,108 | ||
| 1,028 | 1,118 | ||
| 1,038 | 1,129 | ||
| 1,048 | 1,139 | ||
| 1,057 | 1,149 | ||
| 1,067 | 1,174 |
4. Если в таблице нет цифры, соответствующей найденной плотности, то последнюю вычисляют методом интерполяции по двум ближайшим величинам.
Например , плотность раствора HСl равна 1,032 г/мл.
Берут значения плотности больше и меньше измеренной, и соответствующие им концентрации. Находят разности:
При увеличении плотности на 0,01 процентное содержание соляной кислоты увеличивается на 2%. Найденная плотность меньше наибольшего значения на 1,038 - 1,032 = 0,006. Находят процентное содержание, соответствующее плотности 0,006:
Х = (2 · 0,006) : 0,01 = 1,2 (%).
Вычитая эту величину из наибольшего значения, получают искомую величину:
8% - 1,2% = 6,8%.
5. Зная процентное содержание HCl, вычисляют объем концентрированного (исходного) раствора, который необходимо взять для приготовления 0,1N раствора HCl. Объем исходного раствора рассчитывают по формуле:
V – объем концентрированного (исходного) раствора HCl, мл;
С м – молярная концентрация раствора (С м = С N ·f), моль/л;
V к – объем мерной колбы, мл;
М – молекулярная масса вещества, г/моль;
ρ - плотность исходного раствора, г/мл;
ω – процентная концентрация исходного раствора, %.
Например , необходимо приготовить 200 мл 0,1N раствора HCl, тогда
Следовательно, для приготовления 200мл 0,1N (С м = 0,1N·1, т.к. f=1) раствора HCl нужно взять 10,4 мл соляной кислоты плотностью 1,032 г/мл.
5. Мерной пипеткой с точностью до десятых долей мл отмеривают рассчитанный исходный концентрированный раствор HCl, переносят в мерную колбу нужного объема и доводят до метки дистиллированной водой так, чтобы нижний край мениска касался метки.


6. Закрывают колбу пробкой и тщательно перемешивают раствор, переворачивая колбу несколько раз. Полученный таким образом раствор является приблизительно 0,1N. Точная нормальность такого раствора устанавливается с помощью титриметрических анализов.
7. Оформляют работу. Формулируют выводы.
Работа 2. Определение нормальности рабочего раствора HCl
По 0,1N раствору NaOH
Задача работы: ознакомление с методикой титриметрического анализа, т.е. определением концентрации рабочего раствора по титрованному раствору.
Оборудование, реактивы: рабочий раствор HCl, титрованный раствор NaOH, фенолфталеин, коническая колба на 250 мл (или иного объема на усмотрение преподавателя), мерные пипетки, бюретка, груша.
Выполнение работы:
 1. Бюретку заполняют исследуемым рабочим раствором HCl. В титровальную колбу отбирают пипеткой 5 мл 0,1N раствора NaOH, добавляют 1-2 капли фенолфталеина и титруют по каплям раствором кислоты до исчезновения малиновой окраски. При титровании содержимое колбы перемешивают вращательными движениями или магнитной мешалкой.
1. Бюретку заполняют исследуемым рабочим раствором HCl. В титровальную колбу отбирают пипеткой 5 мл 0,1N раствора NaOH, добавляют 1-2 капли фенолфталеина и титруют по каплям раствором кислоты до исчезновения малиновой окраски. При титровании содержимое колбы перемешивают вращательными движениями или магнитной мешалкой.
 2. По шкале бюретки фиксируют расход раствора HCl (V HCl , мл) пошедший на титрование 5 мл NaOH. Титрование повторяют 2-3 раза, каждое повторное титрование начинают с нулевого отсчета бюретки.
2. По шкале бюретки фиксируют расход раствора HCl (V HCl , мл) пошедший на титрование 5 мл NaOH. Титрование повторяют 2-3 раза, каждое повторное титрование начинают с нулевого отсчета бюретки.
По среднему объему кислоты, пошедшему на титрование щелочи рассчитывают ее нормальность по формуле:
![]()
3. Оформляют работу. Формулируют выводы.
Работа 3. Древовидные образования
Задача работы: ознакомление с понятием осмоса и осмотического давления. Изучить сущность явления гемолиза.
 Оборудование, реактивы:
штатив с пробирками, раствор силикатного клея, Кристаллы солей: железа, меди, марганца, никеля, кобальта и др. (хлориды, бромиды, нитраты).
Оборудование, реактивы:
штатив с пробирками, раствор силикатного клея, Кристаллы солей: железа, меди, марганца, никеля, кобальта и др. (хлориды, бромиды, нитраты).
Выполнение работы:
1. Ряд пробирок наполняют раствором силикатного клея и опускают в пробирки кристаллики солей. Через некоторое время из кристаллов вырастают древовидные образования.
2. Дают объяснение наблюдаемому явлению.
| Плотность, г/мл | Массовое содержание, % | Плотность, г/мл | Массовое содержание, % |
| 1,003 | 1,088 | ||
| 1,008 | 1,098 | ||
| 1,018 | … 1,108 |
||
| 1,028 | 1,118 | ||
| 1,038 | 1,129 | ||
| 1,048 | 1,139 | ||
| 1,057 | 1,149 | ||
| 1,067 | 1,174 |
4. Если в таблице нет цифры, соответствующей найденной плотности, то последнюю вычисляют методом интерполяции по двум ближайшим величинам.
Например , плотность раствора HСl равна 1,032 г/мл.
Берут значения плотности больше и меньше измеренной, и соответствующие им концентрации. Находят разности:
При увеличении плотности на 0,01 процентное содержание соляной кислоты увеличивается на 2%. Найденная плотность меньше наибольшего значения на 1,038 — 1,032 = 0,006. Находят процентное содержание, соответствующее плотности 0,006:
Х = (2 · 0,006) : 0,01 = 1,2 (%).
Вычитая эту величину из наибольшего значения, получают искомую величину:
8% — 1,2% = 6,8%.
5. Зная процентное содержание HCl, вычисляют объем концентрированного (исходного) раствора, который необходимо взять для приготовления 0,1N раствора HCl. Объем исходного раствора рассчитывают по формуле:
V – объем концентрированного (исходного) раствора HCl, мл;
С м – молярная концентрация раствора (С м = С N ·f), моль/л;
V к – объем мерной колбы, мл;
М – молекулярная масса вещества, г/моль;
ρ — плотность исходного раствора, г/мл;
ω – процентная концентрация исходного раствора, %.
Например , необходимо приготовить 200 мл 0,1N раствора HCl, тогда
Следовательно, для приготовления 200мл 0,1N (С м = 0,1N·1, т.к. f=1) раствора HCl нужно взять 10,4 мл соляной кислоты плотностью 1,032 г/мл.
5. Мерной пипеткой с точностью до десятых долей мл отмеривают рассчитанный исходный концентрированный раствор HCl, переносят в мерную колбу нужного объема и доводят до метки дистиллированной водой так, чтобы нижний край мениска касался метки.


6. Закрывают колбу пробкой и тщательно перемешивают раствор, переворачивая колбу несколько раз. Полученный таким образом раствор является приблизительно 0,1N. Точная нормальность такого раствора устанавливается с помощью титриметрических анализов.
7. Оформляют работу. Формулируют выводы.
